Mucoviscidose : des organoïdes pour identifier de nouvelles stratégies thérapeutiques antimicrobiennes
Les patients atteints de mucoviscidose souffrent d’infections pulmonaires, première cause de mortalité L’étude des interactions entre l’hôte et les pathogènes associés à cette maladie comme Mycobacterium abscessus (Mabs) permettrait d’identifier des stratégies thérapeutiques antimicrobiennes complémentaires aux traitements antibiotiques. Dans un article publié dans la revue Plos Pathogen, les scientifiques montrent, à l’aide d’organoïdes, que l’activation d’une voie antioxydante, en combinaison avec un antibiotique de première ligne, contribue à un meilleur contrôle de l’infection.
La mucoviscidose est la maladie génétique rare la plus fréquente. Chez ces patients, les infections respiratoires contribuent à la perte de fonction pulmonaire et sont la première cause de mortalité. Parmi les pathogènes associés à la mucoviscidose, les mycobactéries non tuberculeuses comme Mycobacterium abscessus (Mabs) constituent un enjeu thérapeutique majeur de par leur résistance naturelle aux antibiotiques.
Dans cette étude, publiée dans la revue Plos Pathogen, les scientifiques s’appuient sur la technologie des organoïdes pour générer in vitro des mini-poumons sains ou pathologiques. Les organoïdes, obtenus à partir de biopsies de patients, reproduisent in vitro l’architecture et la fonction des voies respiratoires humaines ainsi que les caractéristiques de cette maladie, pour laquelle le modèle murin n’est pas pertinent.
Les résultats montrent que les organoïdes constituent un bon modèle pour reproduire les caractéristiques de l’infection par Mabs, à savoir la formation de biofilms par le variant S (smooth), et de cordes par le variant R (rough). De plus, l’infection par Mabs induit la production d’espèces réactives de l’oxygène et la mort des cellules épithéliales. Au niveau moléculaire, l’infection par Mabs est associée à l’activation de l’axe NRF2-NQO1, régulateur de la réponse antioxydante, dont l’activation par la molécule sulforaphane réduit la charge bactérienne dans les organoïdes. Ainsi, Mabs bénéficie de cet environnement oxydatif pour se développer.
Un des avantages de la technologie des organoïdes est de pouvoir mimer in vitro des pathologies humaines, telle que la mucoviscidose à partir de biopsie de patients. Dans cette étude, les scientifiques montrent que les organoïdes de patients présentent une hyperplasie de l’épithélium, une sécrétion exacerbée de mucus, et un stress oxydatif élevé associé à un défaut d’expression de NRF2, caractéristiques majeures de la mucoviscidose. L’infection des organoïdes de patients avec Mabs conduit à une croissance exacerbée des bactéries, une augmentation du stress oxydatif et de la mort cellulaire, comparativement aux organoïdes sains. Ainsi, l’environnement de la mucoviscidose favorise la croissance et la virulence de Mabs. Dans ce contexte, la restauration de la fonction de l’axe NRF2-NQO1 par le sulforaphane, seul ou en combinaison avec la céfoxitine, antibiotique de première ligne, conduit à un meilleur contrôle de l’infection.
Ainsi, l’activation pharmacologique de la voie NRF2-NQO1 pourrait constituer une approche thérapeutique complémentaire aux antibiotiques pour traiter les patients atteints de mucoviscidose et colonisés par Mabs.
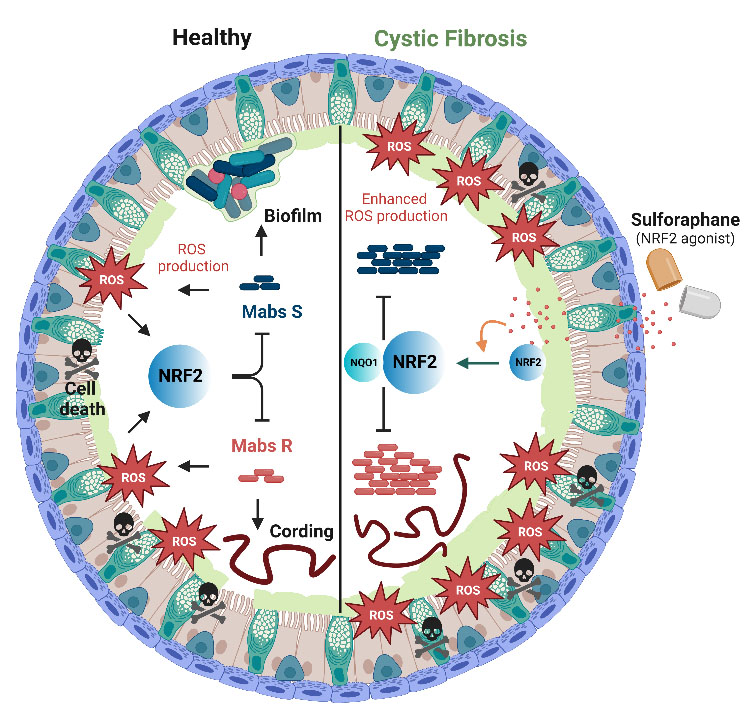
Figure : Mycobacterium abscessus exploite l'environnement oxydatif de la mucoviscidose pour se multiplier.
À l'état basal, les organoïdes sains (H-AOs) et les organoïdes de patients atteints de mucoviscidose (CF-AOs) présentent des compositions cellulaires similaires. Cependant, les CF-AOs présentent des caractéristiques clés de la maladie: accumulation de mucus, stress oxydatif accru et augmentation de la mort cellulaire. Les formes lisses (S) et rugueuses (R) de M. abscessus se répliquent plus efficacement dans les CF-AOs ; les S-M. abscessus forment des biofilms, tandis que les R-M. abscessus forment des cordes, indiquant une virulence plus élevée. Les infections par M. abscessus déclenchent un stress oxydatif accru dans les CF-AOs, exploitant l'environnement pour la croissance. L'activation des voies de détoxification via des agonistes de l’axe NRF2-NQO1, comme le sulforaphane, réduit les ROS et la mort cellulaire dans les CF-AOs, contribuant à un meilleur contrôle de la croissance de M. abscessus.
En savoir plus :
Leon-Icaza SA, Bagayoko S, Vergé R, Iakobachvili N, Ferrand C, Aydogan T, et al. (2023) Druggable redox pathways against Mycobacterium abscessus in cystic fibrosis patient-derived airway organoids. PLoS Pathog 19(8): e1011559. https://doi.org/10.1371/journal.ppat.1011559
Contact
Laboratoire
Institut de pharmacologie et biologie structurale – IPBS (CNRS/Université Toulouse III – Paul Sabatier)
205 route de Narbonne
31400 Toulouse