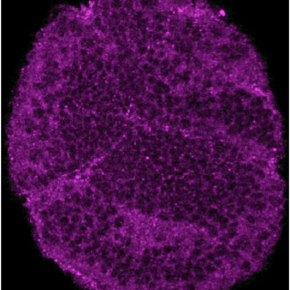
Sobremesa : grand corps, petit cerveau
Une étude publiée dans la revue Cell Reports révèle une voie de signalisation reliant le métabolisme au contrôle du développement. Cette voie régit de façon opposée la croissance du corps et du cerveau. Elle implique un transporteur d'acides aminés (Sobremesa) exprimé dans la glie, cellules du système nerveux dont la fonction est encore mal saisie. Ces données ouvrent des champs d'investigation prometteurs pour comprendre certains événements intervenant dans le développement de l’humain.
Comprendre les divers stades de développement d'un organisme est fondamental dans l’optique de corriger les défauts pouvant survenir à ces moments de la vie. En utilisant la drosophile pour en révéler les acteurs génétiques, les chercheurs ont mis en évidence un transporteur d’acides aminés qu'ils ont nommé Sobremesa (Sbm). En espagnol, « Sobremesa » se réfère aux longues discussions autour d’un bon repas qui s’éternise. Sbm a les caractéristiques biochimiques d’un transporteur d’acides aminés de la famille des SLC7. Cette famille de transporteurs d’acides aminés est suspectée d’être impliquée dans de nombreuses maladies métaboliques et du système nerveux chez l’humain.
Lorsqu'ils perturbent l’expression de ce transporteur chez les larves (stade juvénile), celles-ci restent dans la nourriture et mettent beaucoup plus de temps avant de se métamorphoser en adultes. S'ils inactivent l’expression de Sbm spécifiquement dans les cellules gliales situées dans le cerveau des larves, cela augmente significativement leur durée de développement. Ces larves deviennent ainsi plus grosses, avec des disques imaginaux (tissus participant à la formation de l’adulte) et un corps gras (tissu adipeux) plus gros, mais ont, de façon surprenante, un cerveau plus petit que les larves témoins. Ce petit cerveau chez les larves exprimant moins Sbm présente un retard de développement du système nerveux, possède moins de cellules en division et de cellules gliales.
Les chercheurs ont pu mettre en évidence une partie du mode d’action de ce transporteur d’acides aminés ayant pour origine les cellules gliales des larves. La sous-expression de Sb retarde la survenue d’un pic d’hormone (PTTH) et réduit l’expression de gènes liés à une seconde hormone (ecdysone), allongeant ainsi la durée du stade larvaire juvénile. La voie de l’insuline est également mobilisée mais de façon inattendue. L’ensemble de ces données pourrait permettre de mieux comprendre les maladies liées à la prise alimentaire et à la croissance chez l’Homme, et ainsi apporter de possibles nouvelles stratégies thérapeutiques.
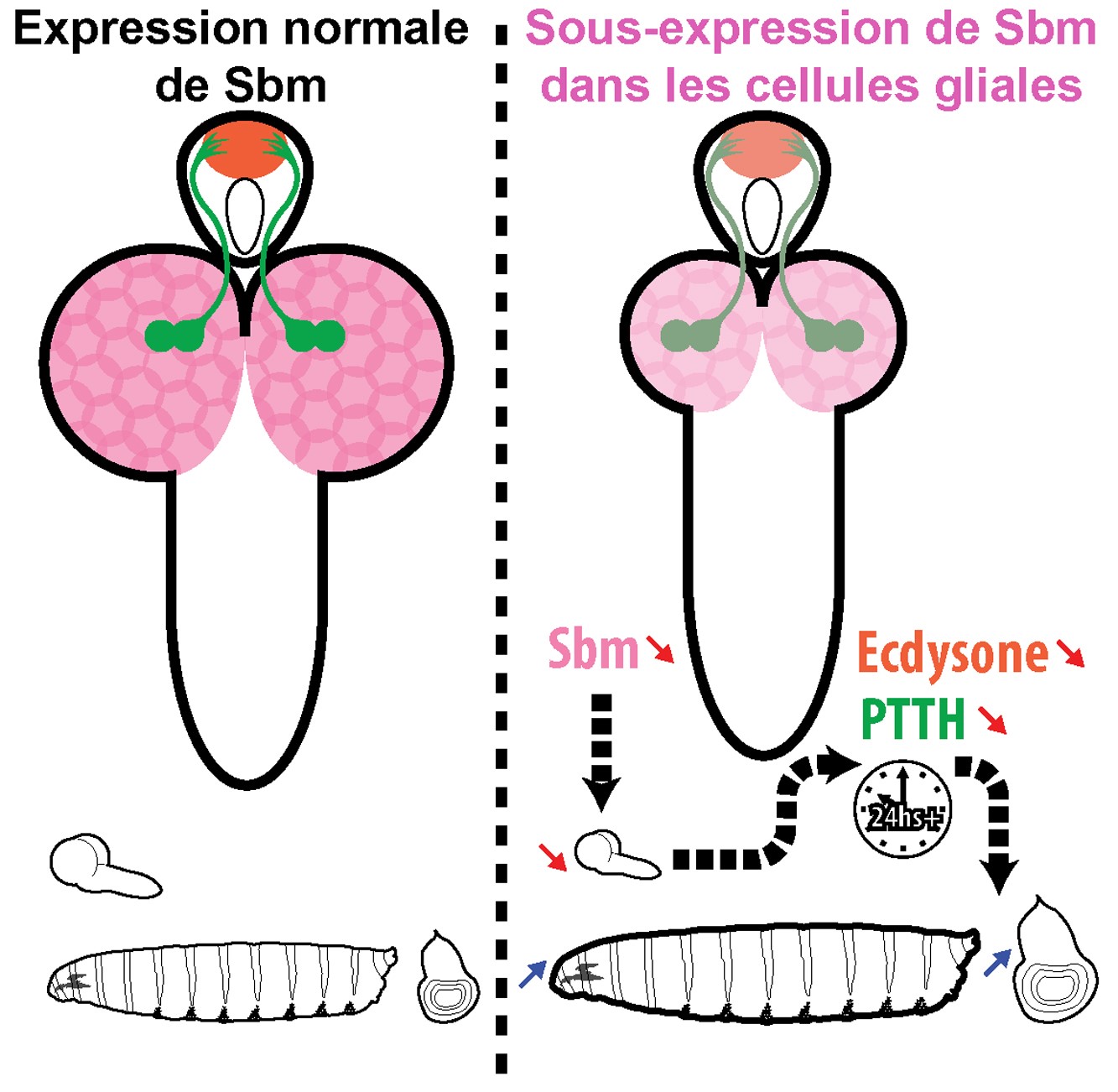
© Diego Galagovsky & Yaël Grosjean (Licence CC BY 4.0)
En savoir plus :
Sobremesa L-type Amino Acid Transporter Expressed in Glia Is Essential for Proper Timing of Development and Brain Growth.
Galagovsky D, Depetris-Chauvin A, Manière G, Geillon F, Berthelot-Grosjean M, Noirot E, Alves G, Grosjean Y.
Cell Rep. 2018 Sep 18;24(12):3156-3166.e4. doi: 10.1016/j.celrep.2018.08.067