Nouvelle stratégie pour l'optimisation des catalyseurs électrochimiques supportés
L'amélioration des performances d'un catalyseur moléculaire peut s'envisager par la modification de sa structure, mais aussi de celle de la matrice qui le supporte, qui peut en changer totalement les propriétés. Dans le cadre d'une collaboration avec l'université de Bochum, les chercheurs montrent que dans des systèmes optimisés, ces effets peuvent prévenir complètement et durablement l'inactivation d'un catalyseur d'oxydation de l'hydrogène par l'oxygène sans compromettre l'efficacité du système. L'approche est particulièrement utile/envisageable dans le contexte des biopiles à combustibles, où le catalyseur sur une des deux électrodes oxyde le dihydrogène, mais peut être inactivé par le dioxygène qui peut traverser la membrane de la fuelcell.
Au cours de travaux antérieurs, le même consortium franco/allemand avait déjà montré qu'une hydrogénase (un catalyseur d'oxydation du dihydrogène très efficace mais très sensible à l'oxygène) peut s'auto-protéger dans un film de polymère rédox épais déposé sur une électrode : l'hydrogène pénètre le film depuis la surface éloignée de l'électrode, une partie est oxydée par le catalyseur près de l'électrode et transformée en courant, et une fraction est oxydée à l'autre extrémité du film, près de la solution, pour produire des électrons qui réduisent le dioxygène et l'empêchent de diffuser dans le film. L'idée que les deux réactions doivent être séparées l'une de l'autre avait conduit à utiliser des films épais (plusieurs centaines de microns), ce qui présentait deux inconvénients majeurs : ce film faisait obstacle à la pénétration du dihydrogène, ce qui avait pour effet de limiter le courant ; et l'immense majorité du catalyseur (>99%) incorporé dans le film ne pouvait pas contribuer au courant.
Ce verrou est maintenant levé grâce à la combinaison de plusieurs avancées majeures. L'observation expérimentale surprenante que des films très fins (de l'ordre de quelques microns) permettent de mieux protéger l'enzyme tout en permettant une plus grande utilisation du catalyseur (jusqu'à 25%) et l'obtention d'un courant plus élevé est parfaitement expliquée par la modélisation des processus de réaction et diffusion à l'intérieur du film. Celle-ci permet de déterminer la limite d'épaisseur en dessous de laquelle le film rédox échoue à protéger l'enzyme, mais aussi de montrer que cette limite peut encore être repoussée en modifiant le catalyseur, non pas pour diminuer sa vitesse d'inactivation, mais en augmentant la vitesse avec laquelle il peut être réactivé par les électrons produits par des enzymes voisines et encore actives. Il a suffi de puiser dans la bibliothèque d'enzymes modifiées par mutagenèse déjà disponibles pour trouver celle qui permet d'illustrer cet effet synergique qui permet à des films très minces (moins de 3 microns) de résister à l'oxygène. Enfin, la modélisation explique comment la vitesse de transfert d'électrons à l'intérieur du film détermine tout à la fois : le courant, la durée de vie du film et son épaisseur minimale ; cette vitesse a pu être augmentée expérimentalement en utilisant des dendrimères rédox parfaitement monodisperses, plutôt que des polymères rédox comme dans les travaux antérieurs.
Ces travaux montrent comment des phénomènes subtils résultant des multiples réactions et couplages avec la diffusion qui se produisent dans l'épaisseur de ces films rédox peuvent modifier - pour le meilleur - les propriétés du catalyseur. Cette stratégie peut être utilisée pour des catalyseurs variés et pourrait aussi être mise en œuvre dans des réactions de réduction (utilisation du CO2, production de dihydrogène) en conditions aérobies.
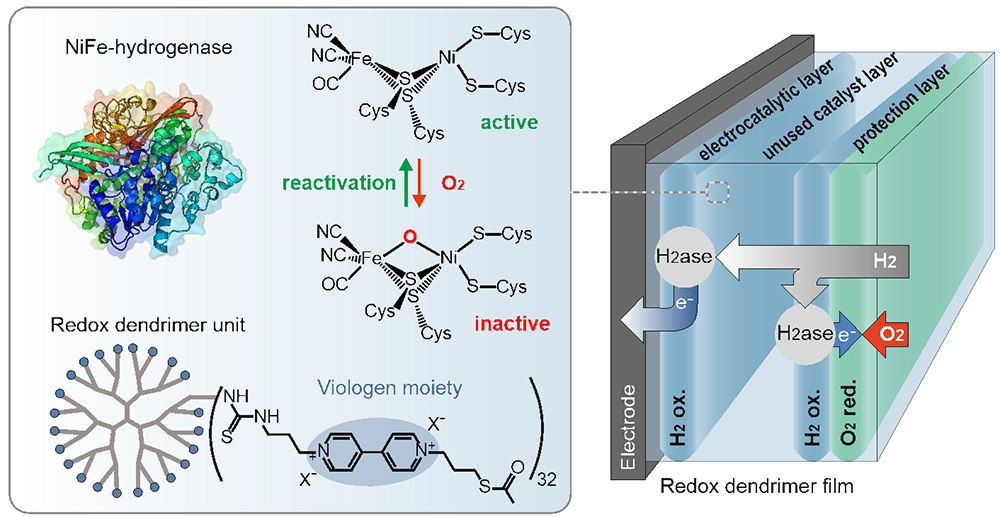
Figure : Illustration des composants et de la structure d'un film de dendrimères rédox déposé sur une électrode et incorporant une hydrogénase sensible à l'oxygène. Des réactions chimiques distinctes se produisent à différentes profondeurs dans le film, permettant l'oxydation du dihydrogène et la production d'un courant d'une part, et d'autre part la réduction du dioxygène, ce qui empêche sa pénétration dans le film.
Pour en savoir plus :
Complete Protection of O2-Sensitive Catalysts in Thin Films
Huaiguang Li, Darren Buesen, Sebastien Dementin, Christophe Leger, Vincent Fourmond, Nicolas Plumere
J. Am. Chem. Soc. 141:42 16734-16742 (2019) doi :10.1021/jacs.9b06790 (open access)
Oxygen Caught on film
David Schilter
Nature Reviews Chemistry (2019) doi : 10.1038/s41570-019-0141-z