L’organisation 3D des génomes dirige l’expression des gènes soumis à l’empreinte
Les maladies liées à des anomalies de l’empreinte parentale sont caractérisées par divers symptômes incluant des altérations de la croissance, des défauts endocriniens et un handicap mental. Dans la revue Genome Biology, les chercheurs montrent que, chez la souris, l’organisation tridimensionnelle des régions chromosomiques contrôle l’expression de gènes qui, chez l’homme, sont impliqués dans ces syndromes complexes.
Chez les mammifères, l’information génétique est portée par deux exemplaires de chaque chromosome, l’un hérité de la mère et l’autre hérité du père. La majorité des gènes s’expriment à des niveaux similaires sur ces deux exemplaires, mais quelques 150 gènes échappent à cette règle. Ces gènes portent un « signal » sur l’une des deux copies chromosomiques qui indique si celle-ci a été héritée du père ou de la mère. Cette marque, qui permet leur distinction, s’appelle une « empreinte parentale ». Cette empreinte, prend la forme d’une modification épigénétique dans l’ADN (la méthylation des acides nucléiques) et régule l’expression de ces gènes. En conséquence, les gènes soumis à l’empreinte parentale acquièrent des patrons d’expression opposés et ne sont de facto exprimés que depuis l’une des deux copies du chromosome. Cependant, il est encore mal compris comment ces modifications épigénétiques dirigent l’expression mono-chromosomique des gènes soumis à l’empreinte parentale.
Quatre syndromes liés à des dysfonctionnements de l’empreinte parentale (les syndromes Beckwith-Wiedemann, Silver-Russell, Kagami-Ogata et Temple) sont causés par des anomalies génétiques ou épigénétiques survenant sur deux larges régions chromosomiques. Ces anomalies entraînent la perte de distinction entre les chromosomes et conduisent à des symptômes divers comme des altérations développementales, une croissance aberrante at des defaults endocriniens. Pour ces deux régions chromosomiques, c’est l’exemplaire hérité du père qui porte l’empreinte de méthylation de l’ADN chez les individus en bonne santé.
Les chercheurs ont montré que le facteur CTCF murin, une protéine essentielle aux repliements des chromosomes sous forme de boucles, possède des sites de fixation plus nombreux sur les deux régions héritées de la mère (où l’empreinte de méthylation est absente).
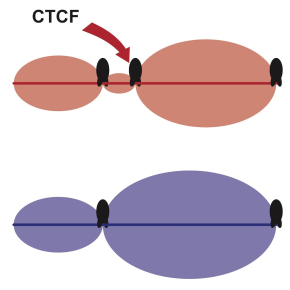
En combinant des approches de génomique et de microscopie à haute résolution, ils démontrent que ces sites additionnels de fixation de CTCF conduisent, sur le chromosome maternel, à la formation de nouveaux « Domaines d’Association Topologique » ou TADs (illustration). Les TADs sont des unités structurales et fonctionnelles des génomes connues pour restreindre les possibilités d’interaction entre gènes et éléments régulateurs, et contribuant ainsi à l’expression des gènes présents au sein du TAD. Cela indique donc que les sites de fixation de CTCF, au niveau de deux régions sujettes à l’empreinte parentale, conduisent à une subdivision des TADs différente sur le chromosome maternel et paternel. Cette différence d’organisation structurelle contrôle en retour l’expression des gènes de la région et conduit à ce que ceux-ci ne soient exprimés que depuis l’un des deux exemplaires, soit le chromosome maternel, soit le chromosome paternel.
Ces découvertes effectuées dans des cellules de souris pourrait améliorer notre compréhension des dérégulations survenant dans les syndromes liés à des anomalies de l’empreinte parentale chez l’homme.
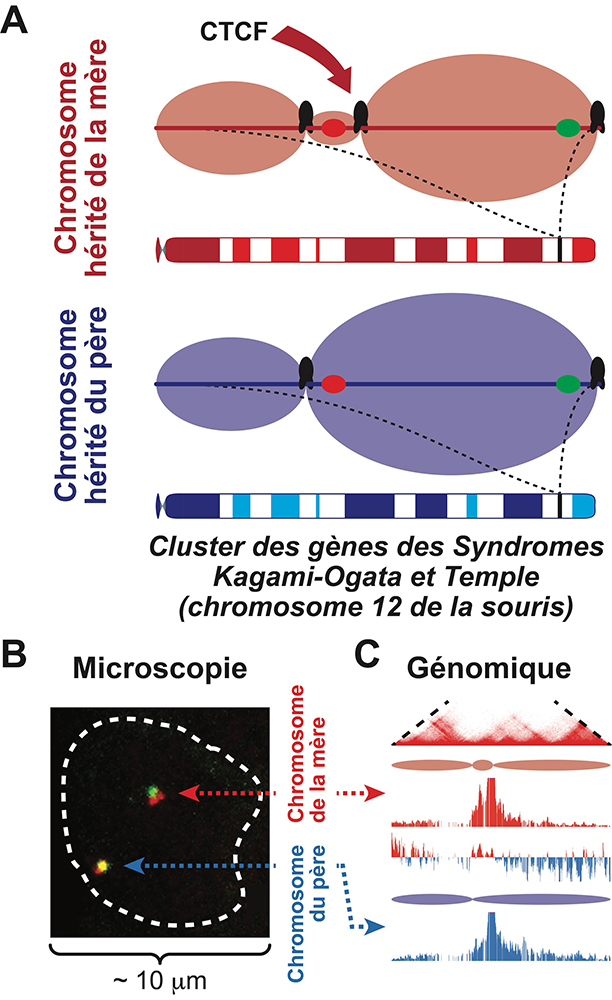
Figure : A. La région chromosomique (ADN) contenant les gènes responsables des syndromes Kagami-Ogata et Temple est séparée en trois domaines structurels (« TADs ») sur le chromosome hérité de la mère, alors que seulement deux domaines sont présents sur le chromosome hérité du père, où un « signal » épigénétique empêche un troisième cas de fixation de la protéine CTCF.
B. Microscopie à haute résolution montrant deux gènes (marqués par un colorant rouge ou vert) séparés sur le chromosome hérité de la mère mais superposés (rouge+vert=jaune) sur le chromosome hérité du père.
C. Approche génomique à haute résolution pour identifier 3 TADs sur le chromosome hérité de la mère et confirmer la fusion de deux TADs sur le chromosome hérité du père.
Pour en savoir plus :
CTCF modulates allele-specific sub-TAD organisation and imprinted gene activity at the mouse Dlk1-Dio3 and Igf2-H19 domains.
Llères D, Moindrot B, Pathak R, Piras V, Matelot M, Pignard B, Marchand A, Poncelet M, Perrin A, Tellier V, Feil R, Noordermeer D.
Genome Biology, 12 December 2019. DOI : 10.1186/s13059-019-1896-8