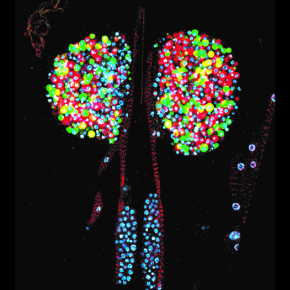
Les macrophages précoces influent sur le fonctionnement des Cellules Souches Hématopoïétiques
Les altérations des macrophages sont impliquées dans de graves roubles fœtaux et néonataux. Dans un article publié dans Developmental Cell, des scientifiques montrent que la déplétion des macrophages précoces, entraînent des changements durables du fonctionnement des Cellules Souches Hématopoïétiques (CSH), chez la mouche comme chez la souris.
En tant que cellules phagocytaires, les macrophages constituent la première ligne de défense contre le non-soi. Outre leur rôle dans l'immunité innée, des preuves de plus en plus nombreuses soulignent l'importance des macrophages dans le développement et l'homéostasie des organes. Les altérations des macrophages sont associées à de graves troubles fœtaux et néonataux (par exemple, troubles du développement neurologique et troubles myéloïdes), ce qui appelle à une meilleure compréhension des fonctions des macrophages au cours du développement.
Les macrophages proviennent de vagues hématopoïétiques distinctes mais qui se chevauchent partiellement. Les macrophages de la vague précoce, produits de façon indépendante des cellules souches hématopoïétiques (CSH), sont présents dans le même micro-environnement, la niche du foie fœtal, où les CSH se développent et se différencient. Les CSH soutiennent le système immunitaire des vertébrés adultes tout au long de leur vie. La population de CSH est établie au cours du développement, sans génération de novo à l'âge adulte. Les perturbations embryonnaires peuvent donc affecter le développement des CSH, entraînant des changements durables dans la capacité des organismes à répondre aux défis immunitaires ultérieurs. Le développement du système immunitaire par vagues successives est conservé tout au long de l'évolution. Chez la drosophile, les macrophages de la première vague ont déjà colonisé la larve au moment où l'hématopoïèse tardive a lieu dans un organe spécifique appelé glande lymphatique. Cela permet de combiner les avantages de deux organismes modèles, le modèle invertébré Drosophila melanogaster et la souris, pour une étude complémentaire et synergique de la contribution des macrophages précoces à l'établissement de l'hématopoïèse tardive.
Dans une étude publiée dans la revue Developmental Cell, des scientifiques montrent que les macrophages de la vague précoce jouent un rôle clé dans la modulation de l'hématopoïèse tardive et que ce rôle est conservé au cours de l'évolution. La déplétion des macrophages de la vague précoce chez la drosophile accélère la maturation de la glande lymphatique et la différenciation des macrophages de la vague hématopoïétique tardive. Ce phénotype ne repose pas sur l'inflammation, ni sur la fonction phagocytaire des macrophages, mais plutôt sur des molécules de la matrice extracellulaire dérivées des macrophages précoces qui assurent une bonne architecture de la glande lymphatique. De même, la déplétion des macrophages de la vague précoce au cours de l'hématopoïèse du foie fœtal chez la souris déclenche une différenciation prématurée des CSH et s'associe à une matrice extracellulaire défectueuse du foie fœtal. Il est important de noter que l'épuisement transitoire des macrophages précoces entraîne des changements durables dans les CSH adultes, avec un potentiel myéloïde accru aux dépens des progéniteurs lymphoïdes.
Ces résultats augmentent les connaissances actuelles sur les fonctions homéostatiques des macrophages et dévoilent un lien, jusqu'à présent inexploré, entre les vagues hématopoïétiques. Cela ouvre des perspectives importantes en sciences fondamentales et médicales, avec le rôle potentiel de l'hématopoïèse précoce dans la formation du système immunitaire adulte, influençant ainsi le risque de développer des maladies après la naissance.
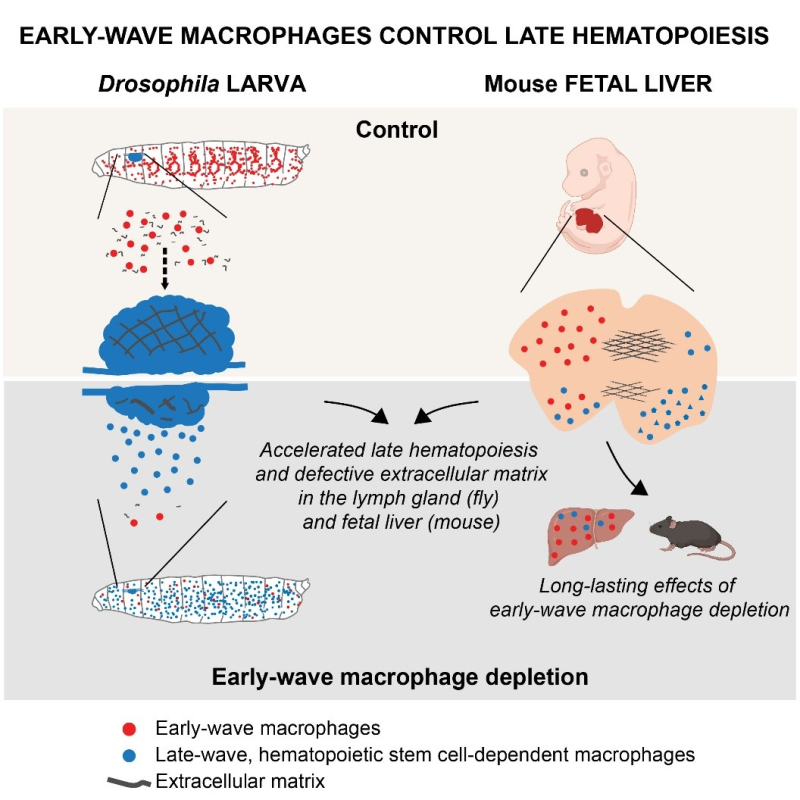
Figure : Schématique des résultats obtenus. La déplétion des macrophages précoces accélère la vague hématopoïétique tardive chez la drosophile et la souris.
Pour en savoir plus :
Early-wave macrophages control late hematopoiesis
Monticelli, S., Sommer, A., AlHajj Hassan, Z., Garcia Rodriguez, C., Adé, K., Cattenoz, P., Delaporte, C., Gomez Perdiguero, E., & Giangrande, A. (2024). Developmental cell, S1534-5807(24)00182-5. https://doi.org/10.1016/j.devcel.2024.03.013
Contact
Laboratoires
Institut de génétique et de biologie moléculaire et cellulaire - IGBMC (CNRS / Inserm / Université de Strasbourg)
1 Rue Laurent Fries
67404 ILLKIRCH CEDEX
Département biologie du développement et cellules souches (CNRS / Institut Pasteur)
25-28 rue du Docteur Roux
75724 PARIS CEDEX 15