L’axone suit un chemin balisé pour rejoindre sa cible musculaire
Les neurones moteurs, dans la moelle épinière, émettent, au cours du développement, des prolongements, les axones, qui doivent se frayer un chemin vers les cellules musculaires. Dans un article publié dans la revue PNAS, des biologistes en utilisant le poisson zèbre démontrent l’existence de deux protéines qui, telles les balises rouges et vertes à l’entrée d’un port, guident le trajet de l’axone. Bioimprimé, ce duo protéique s’avère fonctionnel, ouvrant des perspectives prometteuses pour la régénération de nerfs endommagés.
Le système locomoteur représente un ensemble de tissus et organes qui, par leur connexion étroite, confère aux organismes la capacité de se mouvoir physiquement, notamment par l’intermédiaire des nerfs moteurs. Les motoneurones présents dans la moelle épinière et qui forment les nerfs sont des cellules spécialisées dans la commande du mouvement et représentent le dernier relai entre signal électrique et signal mécanique. Par l’intermédiaire de leurs axones, ils déclenchent le mouvement.
Les axones moteurs ont besoin de signaux pour rejoindre leur cible, la cellule musculaire.
Pendant le développement embryonnaire, l’ensemble du système locomoteur se met en place avec une précision spatiotemporelle fascinante. Le développement des axones moteurs illustre parfaitement cette dynamique. En route vers leurs cibles musculaires, les axones moteurs suivent une trajectoire stéréotypée, guidés par une combinaison de signaux moléculaires qui leur permet d’atteindre avec précision leur cible et de se connecter via la formation de synapses. De façon remarquable, ce même chemin sera emprunté par les axones moteurs au cours de la régénération en cas de section accidentelle d’un nerf.
C’est l’extrémité distale de l’axone, sorte de « tête chercheuse » du motoneurone appelé cône de croissance, qui interprète ces signaux de guidage, qu’ils soient attractifs ou répulsifs pour guider l’axone en croissance. Les molécules de guidage les plus étudiées sont celles qui sont distribuées sous forme d’un gradient dans l’environnement de l’axone. La navigation des axones est aussi influencée localement par des protéines sécrétées qui vont être déposées le long du chemin axonal et immobilisées à cet endroit. Ces signaux agissent comme de véritables panneaux de signalisation en pavant la trajectoire des axones balises rouges et vertes et en guidant les axones comme un navire vers son port de destination.
Deux protéines sont déposés par les progéniteurs musculaires pour guider les axones.
Le répertoire, l’organisation et la fonction de ces signaux de contact, ainsi que leur source cellulaire, restent un champ d’investigation largement ouvert. Les protéines sécrétées qui composent l’environnement immédiat de pratiquement tout type de cellules s’organisent en réseau complexe, appelé matrice extracellulaire. Chaque réseau est spécifique d’un tissu ou d’un organe. Par sa composition, son organisation et ses propriétés mécaniques, la matrice extracellulaire influence le comportement des cellules tout au long de leur vie. La cellule est à la fois auteure, lectrice et interprète de ces réseaux. Dans cet article, publié dans la revue PNAS, les scientifiques se sont intéréssés à décoder le trio fonctionnel : identité, configuration dans l’espace (topologie) et fonction en tant que signaux de guidage. Ils ont utilisé le poisson-zèbre, petit vertébré tropical allié des biologistes du développement, pour démontrer que des progéniteurs musculaires en cours de différenciation produisent et déposent le long du futur chemin axonal, une centaine de protéines de la matrice extracellulaire (défini comme le « matrisome » de ces cellules), quelques heures seulement avant la sortie des axones de la moelle épinière. Ces travaux mettent en évidence un processus complexe où deux protéines de la matrice extracellulaire, le Collagène XV et la Ténascine C, sont déposées de manière séquentielle le long du chemin axonal par ces progéniteurs, dans un jeu subtil entre dimensions spatiale et temporelle. Cette séquence conduit à la formation d’un chemin central tapissé de Collagène XV qui agit comme un signal « go » en modulant la rigidité de la voie, qui sous l’influence directe du Collagène XV, est borné de part et d'autre par un dépôt de Ténascine C, signal « stop » pour l’axone. Leur absence au cours du développement cause des défauts de navigation, un arrêt de croissance et une arborisation aberrante des axones moteurs.
Avec un intérêt particulier pour la médecine régénératrice des nerfs, nous avons alors bio-imprimé un chemin mimant fidèlement celui observé in vivo. Nous avons ainsi démontré que les axones moteurs isolés, placés en présence de ces micro-patterns, suivent précisément le chemin tracé par les signaux « go » du Collagène XV et se détournent des bornes « stop » formées par la Ténascine C. Ces résultats ouvrent la voie à des applications en médecine régénérative, notamment dans les situations où la lésion est trop étendue pour permettre une régénération complète des nerfs.
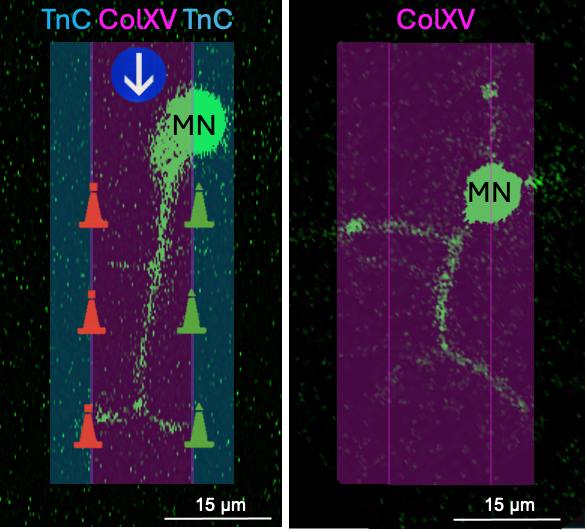
Figure : Les motoneurones (en vert) isolés à partir d'embryons de la lignée fluorescente de poisson zèbre (mnx1:gfp) et placés sur un support bio-imprimé qui imite la topologie des protéines matricielles observée in vivo : à gauche, le collagène XV (ColXV, magenta) au centre oriente la navigation, il est borné par la Ténascine C (TnC, cyan) qui balise le chemin des axones. A droite, en l'absence de balise, l'axone perd son cap et navigue à vue.
En savoir plus : Nemoz-Billet L, Balland M, Gilquin L, Gillet B, Stévant I, Guillon E, Hughes S, Carpentier G, Vaganay E, Sohm F, Gonzalez-Melo M-J, Koch M, Ghavi-Helm Y, Bretaud S and Ruggiero F (2024) Dual-topology of collagen XV and tenascin C acts in concert to guide and shape developing motor axons. Proc Natl Acad Sci USA. https://www.pnas.org/doi/10.1073/pnas.2314588121
Contact
Laboratoire
Institut génomique fonctionnelle de Lyon - IGFL (CNRS/ENS de Lyon)
32-34 Avenue Tony Garnier
69007 Lyon
