La mécano-biologie décryptée par microscopie de super-résolution
Les cellules s'adaptent et répondent à une multitude de stimuli mécaniques. Cependant, les mécanismes moléculaires de la mécanosensibilité cellulaire sont encore méconnus. Les scientifiques ont réussi à étudier, pour la première fois dans des cellules vivantes, les réponses mécaniques des protéines au sein de structures mécanosensibles. Pour ce faire, là où aucune technologie ne le permettait auparavant, les chercheurs ont combiné les techniques de microscopie de super-résolution et d’étirement cellulaire dans un dispositif miniaturisé innovant. Ces travaux ont été publiés dans la revue Nature Cell Biology.
Les tissus et les cellules d’un organisme sont continuellement soumis à des forces mécaniques. Par exemple, les muscles et les neurones sont étirés pendant le mouvement, le battement du cœur ou la respiration. De façon plus générale, les cellules sondent constamment les propriétés mécaniques de leur microenvironnement, à l’aide de structures adhésives et leur cytosquelette. Cette mécanosensibilité cellulaire joue un rôle clé dans la vie de la cellule car elle régule sa migration, mais aussi sa prolifération et sa mort lors de phénomènes physiologiques tels que le développement. L'altération de cette mécanosensibilité cellulaire est impliquée dans le développement de multiples pathologies, notamment le cancer.
Des études antérieures réalisées sur des protéines purifiées ont montré que la mécanosensibilité cellulaire repose sur la déformation et la réorganisation des protéines. Le consensus général est qu'un stress mécanique externe appliqué aux cellules est directement et instantanément transmis aux protéines au sein des structures adhésives et du cytosquelette. Cependant, cette hypothèse n'a jamais pu être vérifiée car aucune méthode ne permettait auparavant d'appliquer des forces externes aux cellules tout en capturant la réponse mécanique des protéines individuelles au sein de structures cellulaires.
Dans cette étude, les scientifiques ont révélé pour la première fois la réponse mécanique des protéines individuelles en combinant l’étirement cellulaire sur des substrats élastiques avec la microscopie de super-résolution. Les techniques dites de super-résolution (prix Nobel de chimie 2014) permettent de résoudre les structures cellulaires à l'échelle nanométriques et de suivre en direct les mouvements des protéines. Lors d’un étirement cellulaire, certaines protéines, en particulier les protéines d’adhésion, suivent le déplacement élastique du substrat. D’autres, comme les protéines connectées au cytosquelette, ont un comportement inélastique, car elles continuent à être déformées alors même que le substrat n'est plus étiré. Ces déformations moléculaires différées et amplifiées par rapport au stress mécanique initial sont déclenchées par un remodelage transitoire et actif de la machinerie contractile de la cellule composée de filaments d’actine et de moteurs moléculaires. Ces déformations protéiques, qui révèlent des sites d'interaction cachés, permettent le recrutement de nouvelles protéines au sein des structures adhésives.
Les résultats obtenus démontrent que la réponse mécanique des protéines n’est pas obligatoirement déclenchée par une transmission directe des forces externes. Au contraire, une contrainte mécanique externe déclenche une réponse active et déphasée de la cellule. Ce mécanisme amplifie les stimuli mécaniques faibles pour déformer ou recruter des protéines lors de la mécanosensibilité cellulaire.
La combinaison de l'étirement cellulaire et de la microscopie de super-résolution permettra de déchiffrer les mécanismes moléculaires à la base du fonctionnement d’autres structures mécanosensibles tels que la membrane cellulaire ou le noyau.
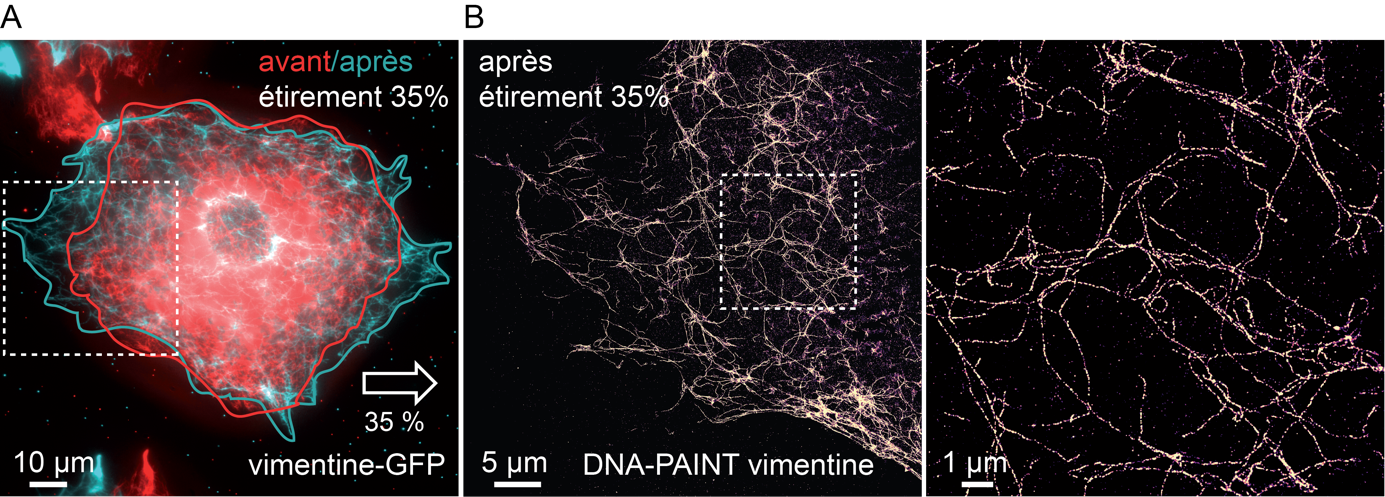
Figure : Ces images des filaments intermédiaires à une résolution d’une dizaine de nanomètres ont été obtenues grâce à une méthode innovante combinant étirement cellulaire (A) et les techniques de microscopie de super-résolution (B). Cette approche permet d’étudier les réponses mécaniques de protéines individuelles au sein des structures mécanosensibles cellulaires.
Pour en savoir plus:
Cell stretching is amplified by active actin remodeling to deform and recruit proteins in mechano-sensitive structures.
Massou S,Nunes Vicente F, Wetzel F, Mehidi A,Strehle D, Leduc C, Voituriez R, Rossier O, Nassoy P, Giannone G.
Nature Cell Biology 27 July 2020. https://doi.org/10.1038/s41556-020-0548-2
Contact
Laboratoires
Institut Interdisciplinaire de NeuroSciences (IINS) - (CNRS/Université de Bordeaux)
Centre Broca Nouvelle-Aquitaine
146 rue Léo-Saignat,
CS 61292 CASE 130, 33076 Bordeaux cedex, France
Institut d’Optique d’Aquitaine, Laboratoire Photonique, Numérique et Nanosciences (LP2N) - (CNRS/Université de Bordeaux)
1 rue François Mitterrand,
F-33405 Talence, France