Infections virales : amies ou ennemies ?
Les infections, même asymptomatiques, peuvent modifier le fonctionnement de notre système immunitaire, voire, parfois, améliorer le cours de maladies inflammatoires concomitantes. Les scientifiques ont analysé ces mécanismes au cours d’une infection virale chez la souris. Dans deux modèles de maladies inflammatoires (sclérose en plaques et neuropaludisme), ils ont montré qu’en ‘neutralisant’ la fonction de certaines cellules immunitaires à l’origine de ces pathologies, la réponse initiale des animaux contre le virus joue un rôle bénéfique. Cette étude est publiée dans la revue mBio.
Tout au long de notre vie, l’exposition à des microorganismes infectieux, qu’ils causent des symptômes ou non (flore commensale, infection asymptomatique, …), peut modifier notre susceptibilité à développer des maladies inflammatoires. Par exemple, des parasites nématodes de type helminthes atténuent la sévérité de certaines maladies autoimmunes. Cette notion est à la base de l’hypothèse hygiéniste qui tente d’expliquer la corrélation inverse observée entre incidence des maladies infectieuses et incidence des maladies autoimmunes. A l’inverse, des virus peuvent aggraver la sévérité d’infections parasitaires, telles que la leishmaniose.
Les chercheurs ont analysé les mécanismes de modulation immunitaire dans le contexte d’une infection par un virus enveloppé à ARN, le LDV, appartenant à l’ordre des Nidovirales qui comprend aussi les coronavirus. Chez la souris, ce virus cause une infection asymptomatique et est capable de persister durablement dans le sang. Ils ont observé que l’infection par ce virus est protectrice dans deux modèles d’immunopathologie dans lesquels les lymphocytes T jouent un rôle néfaste : i) dans le cas d’une co-infection avec Plasmodium, le parasite du paludisme, le LDV prévient le développement d’une complication causée par l’accumulation de lymphocytes T dans les microvaisseaux sanguins cérébraux (neuropaludisme) ; ii) dans un modèle murin de sclérose en plaques, une maladie autoinflammatoire et neurodégénérative, le virus empêche l’apparition des signes cliniques de la maladie.
Les expériences ont montré que l'infection par le LDV induit de fortes réponses immunitaires innées impliquant les interférons de type I à l’origine de défauts quantitatifs et qualitatifs des cellules dendritiques (cellules sentinelles impliquées dans l’induction des réponses médiées par les lymphocytes T). Les cellules dendritiques ainsi ‘conditionnées’ par le virus se retrouvent incapables de transmettre certains signaux instructeurs, dits de ‘polarisation’, aux lymphocytes T CD4+, qui ne sont plus capables de causer ces deux pathologies inflammatoires. Cette activation incomplète des lymphocytes T CD4+ est donc à l'origine de l’effet bénéfique du virus.
Ce travail met en lumière des bases moléculaires et cellulaires par lesquelles une infection virale apparemment anodine peut modifier l'état du système immunitaire d'un individu, avec des répercussions majeures, dans ce cas bénéfiques, sur des maladies inflammatoires. Une meilleure compréhension de ces mécanismes pourrait ouvrir la voie à de nouvelles thérapeutiques s'appuyant sur les voies moléculaires mises en jeu ou les molécules potentiellement immunomodulatrices produites par les pathogènes eux-mêmes.
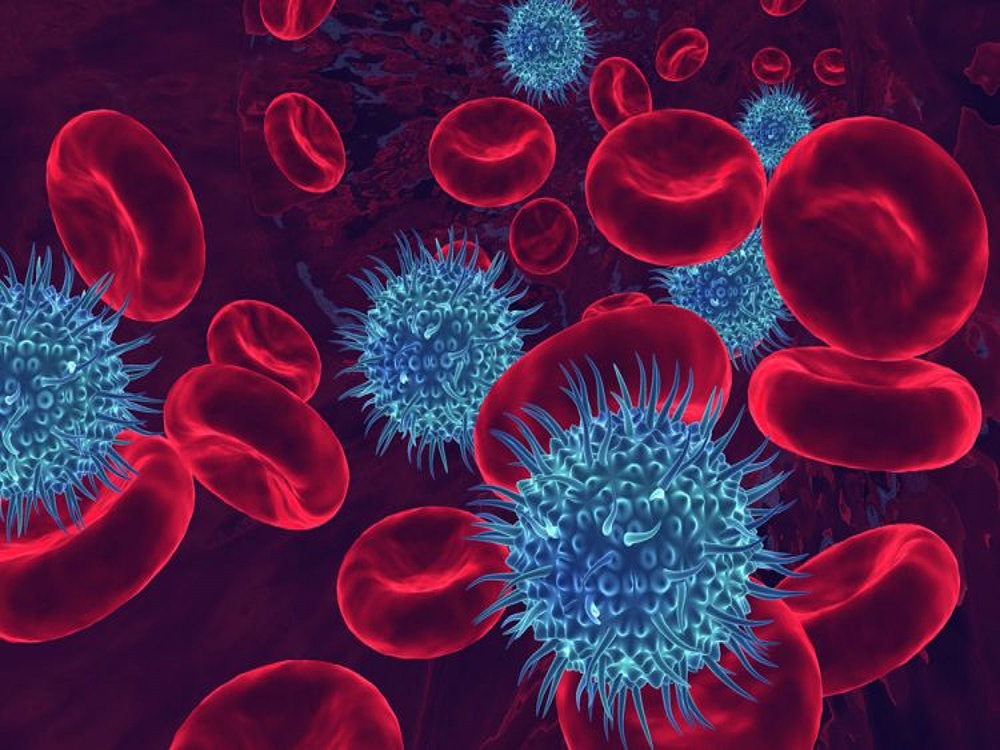
Figure : des virus enveloppés au contact des globules rouges dans la circulation sanguine
Pour en savoir plus:
A Virus Hosted in Malaria-Infected Blood Protects against T Cell-Mediated Inflammatory Diseases by Impairing DC Function in a Type I IFN-Dependent Manner.
Hassan A, Wlodarczyk MF, Benamar M, Bassot E, Salvioni A, Kassem S, Berry A, Saoudi A, Blanchard N.
mBio. 2020 Apr 7;11(2). pii: e03394-19. doi: 10.1128/mBio.03394-19.
Contact
Laboratoire
Centre de Physiopathologie Toulouse Purpan (CPTP) - (Inserm / CNRS / Université de Toulouse)
CHU Purpan, BP3028, 31024 Toulouse Cedex 3