Dénouer l’ADN : quand les ligands de G4 s’en mêlent
Dans cette étude publiée dans la revue eLife, les scientifiques dévoilent le mécanisme de la cytotoxicité de deux ligands des structures particulières adoptées par l’ADN, les G-quadruplexes (G4). En utilisant des approches génétiques et moléculaires originales ils démontrent que deux ligands stabilisant ces structures provoquent des cassures de l’ADN via la Topoisomérase 2A.
L’ADN peut adopter des structures non canoniques, différentes de la double-hélice. Parmi ces structures, les G-quadruplexes (G4) sont des structures à quatre brins formées par des séquences riches en guanines. Les G4 contrôlent la réplication, la transcription des oncogènes et l’activité télomérase, trois processus clés de la tumorigenèse. Ainsi, les G4 sont considérés comme des cibles thérapeutiques anti-cancéreuses potentielles. Ils font l’objet d’un intérêt particulier depuis le début des années 2000 notamment grâce au développement de petites molécules, les ligands de G4, qui les fixent et les stabilisent au sein des cellules. Il était connu que certains ligands de G4 induisent des cassures de l’ADN, expliquant leurs effets cytotoxiques, mais les mécanismes de formation de ces cassures restaient énigmatiques.
Une étude récente a permis de clarifier comment les ligands de G4 induisent des cassures de l’ADN. Elle repose sur l’obtention et le séquençage de cellules résistantes à la toxicité des ligands de G4. Cette approche a révélé que les cassures induites par les ligands de G4 dépendent de la transcription et sont induites par la topoisomérase 2 alpha (TOP2A). La TOP2A est une protéine essentielle, surexprimée dans de nombreux cancers et permettant de résoudre les enchevêtrements d’ADN induits au cours de la transcription et de la réplication de l’ADN. Pour ce faire, la TOP2A coupe les enchevêtrements de l’ADN en induisant une cassure transitoire qu’elle répare aussitôt une fois l’ADN dénoué. Les scientifiques ont découvert que les ligands de G4 bloquent l’activité de la TOP2A au stade de la fermeture de ces cassures transitoires, agissant en « poison » de topoisomérase, selon le même mode que d’autres molécules actuellement utilisées en thérapie anticancéreuse. Toutefois, à la différence de ces dernières, les ligands de G4 empoisonnent sélectivement la TOP2A au niveau des structures G4, agissant par un double mécanisme. Ces travaux ont ainsi permis d’élucider l’activité de la molécule CX-5461, actuellement en évaluation clinique comme anticancéreux.
Une étude parallèle (https://doi.org/10.1038/s41598-021-92806-8), révèle que le complexe NELF s’associe aux G4. Ce complexe est normalement impliqué dans l’arrêt transitoire de la transcription au niveau de sites dits de « pause ». Suspectant que cette association aux G4 avait un impact fonctionnel, les auteurs ont découvert que le complexe NELF est nécessaire à l’induction des cassures de l’ADN par les ligands de G4, indiquant que ces cassures sont liées à l’arrêt de la machinerie de transcription sur des sites de pauses.
Ces deux études permettent donc de mieux comprendre les mécanismes qui déterminent l’efficacité anticancéreuse des ligands de G4 et pourraient aider à orienter de potentielles stratégies thérapeutiques.
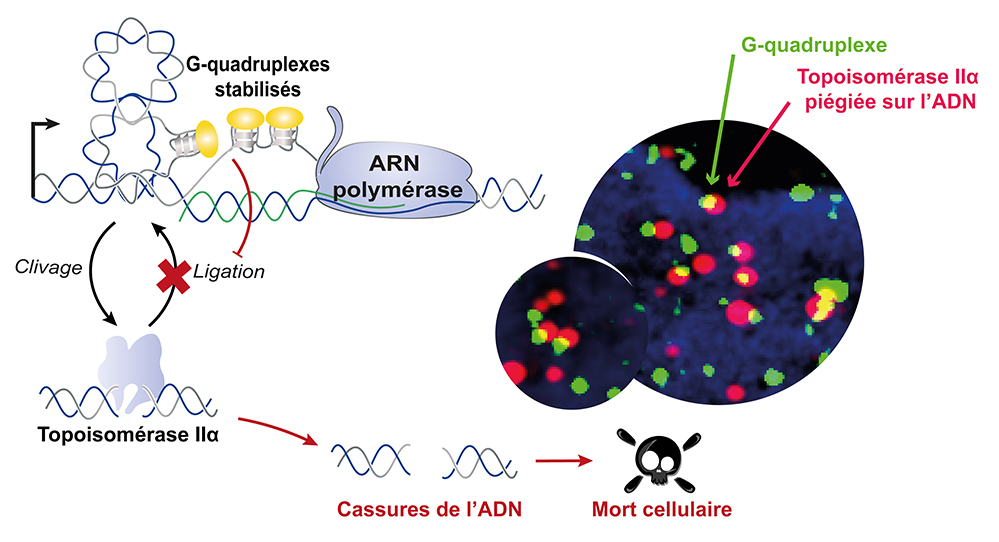
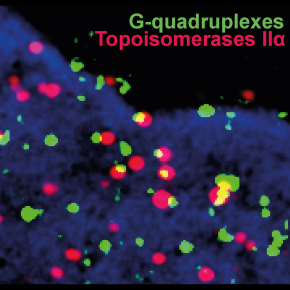
Figure : La stabilisation des structures G-quadruplex formées lors de la transcription provoque des cassures double brin de l’ADN induites par l’activité de la TOP2A selon un mécanisme qui implique l’inhibition de son activité de religature. Cette image de microscopie à haute résolution montre la co-localisation (en jaune) des complexes empoisonnés de TOPO2A (en rouge) avec les structures G-quadruplex (en vert) au sein des cellules humaines.
Pour en savoir plus :
Transcription-associated topoisomerase 2 (TOP2A) activity is a major effector of cytotoxicity induced by G-quadruplex ligands
Bossaert M., Pipier A., Riou J.F., Noirot C., Nguyễn L-T., Serre R-F., Bouchez O., Defrancq E., Calsou P., Britton S., Gomez D.
eLife 28 juin 2021; DOI: 10.7554/eLife.65184
Contact
Laboratoire
Institut de pharmacologie et biologie structurale IPBS-Toulouse (CNRS/Université Paul sabatier)
BP 64182
205 route de Narbonne
31077 Toulouse Cedex 04