Cardiomyopathies, l’origine mécanistique de la maladie enfin comprise grâce à la microscopie électronique
Les cardiomyopathies hypertrophiques, caractérisées par une hypertrophie du cœur, sont les maladies génétiques cardiaques les plus communes. Elles sont causées par des mutations qui touchent principalement la myosine cardiaque, le moteur moléculaire responsable des contractions du cœur. En dévoilant la structure de la myosine cardiaque à l’échelle atomique, les scientifiques dans un article publié dans la revue Nature Communications, expliquent comment des mutations génétiques peuvent perturber la régulation du cœur.
Le cœur est un muscle strié, il est constitué d’unités fondamentales appelées sarcomères. Les sarcomères sont constitués de filaments épais comportant des moteurs moléculaires appelés myosines et de filaments fins d’actine. Lors d’un battement de cœur, les sarcomères se raccourcissent et le muscle se contracte. Les têtes de myosines interagissent avec les filaments d’actine et convertissent l’énergie chimique en énergie mécanique, provoquant ainsi le glissement des filaments d’actine sur les filaments de myosine et le raccourcissement du sarcomère. Afin de réguler la puissance des contractions, une partie de la population de myosines est maintenue dans un état auto-inhibé où deux têtes interagissent l’une avec l’autre, ce qui les empêche d’interagir avec le filament d’actine et de produire de la force. Lors d’un effort intense, cette réserve de myosines inactives peut être recrutée afin d’augmenter la puissance et la fréquence des battements cardiaques.
Dans le contexte pathologique des cardiomyopathies hypertrophiques, des mutations génétiques déstabilisent l’état auto-inhibé, il y a donc une plus grande quantité de myosines actives. Un cœur malade produira donc plus de force à chaque contraction et au fil des années développera une fibrose, et un épaississement des parois de l’organe se produira. Ceci perturbera son fonctionnement, notamment lorsque la voie de sortie du sang est obstruée par cet épaississement. Les symptômes causés par les cardiomyopathies hypertrophiques sont l’essoufflement, les palpitations cardiaques, des douleurs dans la poitrine (angine) et dans les cas les plus sévères un arrêt cardiaque et la mort du patient. Les causes de ces maladies étant méconnues, les traitements des formes graves sont aujourd’hui la transplantation cardiaque ou l’implantation de dispositifs de type pacemaker.
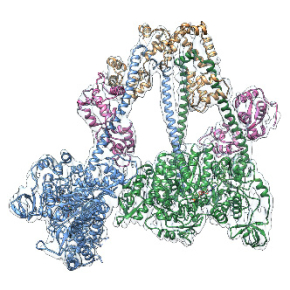
Dans un article publié dans la revue Nature Communications, les scientifiques ont visualisé la structure à haute-résolution de l’état auto-inhibé de la myosine cardiaque par cryo-microscopie électronique. Ils ont ainsi pu constater que les mutations responsables de l’hypertrophie du cœur bloquent l’interaction entre les deux têtes de myosines et empêchent ainsi leur inhibition. Diverses théories ont été avancées depuis les années 1990 pour expliquer le développement des cardiomyopathies hypertrophiques et l’absence de structure de l’état auto-inhibé était le principal frein à l’étude de ces hypothèses. Ils ont en outre démontré que cet état de la myosine cardiaque diffère grandement de celui du muscle lisse, ce qui était complètement inattendu et permet de mieux comprendre comment chaque muscle a évolué afin de pouvoir accomplir des fonctions spécifiques.
L’observation de cette structure est une avancée majeure dans la compréhension de la physiologie du muscle cardiaque et des myosines en général. Ces données permettent d’envisager une nouvelle définition des pathologies cardiaques mais également la conception de nouveaux traitements contre les cardiomyopathies.
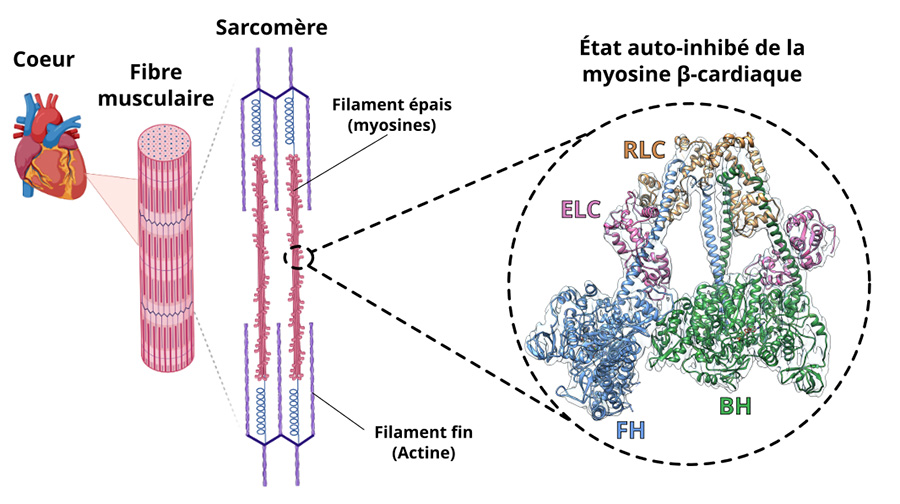
Figure : La structure de l’état auto-inhibé de la myosine cardiaque à haute résolution. Le cœur est un muscle constitué de fibres musculaires. L’unité fondamentale de ces fibres est appelée sarcomère et comporte des filaments de myosines (filaments épais) et des filaments d’actine (filaments fins). L’interaction entre ces deux filaments permet la contraction. Afin de réguler les contractions et éviter toute déperdition d’énergie, une partie des myosines est maintenue dans un état « auto-inhibé » : tête bloquée (BH, blocked head) ; tête libre (FH, free head), chaînes légères (essential light chain, ELC et regulatory light chain, RLC). La structure de cet état a été obtenue à haute-résolution par des scientifiques du CNRS.
Pour en savoir plus :
Cryo-EM structure of the folded-back state of human β-cardiac myosin.
Grinzato A, Auguin D, Kikuti C, Nandwani N, Moussaoui D, Pathak D, Kandiah E, Ruppel KM, Spudich JA, Houdusse A, Robert-Paganin J. Nat Commun. 2023 May 31;14(1):3166. DOI: 10.1038/s41467-023-38698-w.
Contact
Laboratoire
Institut Curie (Paris Université Sciences et Lettres / Sorbonne Université / CNRS)
26, rue d’Ulm
F-75005, Paris